Создатель теории электролитической диссоциации

Сванте Аррениус успешно продолжил электрохимические исследования Фарадея, Берцелиуса и других химиков и разработал теорию электролитической диссоциации, которая в значительной мере способствовала формированию физической химии как науки.
Сванте Август Аррениус (Svante August Arrhenius) родился 19 февраля 1859 года в усадьбе Вейк близ Упсалы. Он был вторым сыном Каролины Кристины (Тунберг) и Сванте Густава Аррениуса, управляющего имения Вейк. Предки Аррениуса были фермерами. Детские и юношеские годы Аррениуса прошли в городе Упсала, где отец Аррениуса вошёл в состав совета инспекторов Уппсальского университета.
Сванте рано начал читать, в шестилетнем возрасте помогал отцу в расчётах. Чтобы дать сыну начальное образование, отец нанял студента - богослова, оказавшегося столь фанатичным и строгим, что Сванте на всю жизнь сохранил неприязнь к религии.
С восьми лет Сванте учился в частной упсальской школе, затем перешёл в реальную гимназию, в которой впервые с большим интересом изучал физику и математику. Весной 1876 г. он получил в гимназии аттестат зрелости и поступил в университет. Впоследствии он жаловался, что обучение в университете велось по устаревшим схемам: например, "нельзя было услышать ни единого слова о менделеевской системе, а ведь ей было уже больше десяти лет"...

В 1878 году он получил степень бакалавра естественных наук, а затем в течение ещё трёх лет продолжал изучать там физику.
После университета он был хорошо подготовлен к научной работе: владел знаниями в области физики, химии, математики, в совершенстве знал английский, немецкий, и французский языки.
Аррениус создал свой стиль работы. Например, он делал далеко идущие выводы на основании небольшого количества экспериментов.
Аррениус не отрицал необходимости проведения экспериментов, но работа только в лаборатории не могла его удовлетворить. Эксперимент он использовал для того, чтобы сделать обобщающие выводы или предложить гипотезы.
В 1881 году переехал в Стокгольм и продолжил обучение в Физическом институте Королевской шведской Академии Наук под руководством физика Эрика Эдлунда. Там Аррениус специализировался в изучении проводимости электролитов, занимался изучением электропроводности сильно разбавленных водных растворов.

Результаты исследований он оформил в виде стопятидесятистраничной докторской диссертации, где уже содержались основные положения электролитической диссоциаций. Привычные в наши дни представления, что соли, кислоты и основания в водном растворе находятся в большей или меньшей степени в виде свободно движущихся ионов, по мнению химиков того времени, ниспровергали все ранее существовавшие взгляды. Поэтому вначале почти все учёные принимали теорию Аррениуса весьма сдержанно. Некоторые даже считали её бессмыслицей. Не удивительно, что диссертация получила плохие отзывы.
В то время физическая природа электричества оставалась неизученной. В частности, было неизвестно, почему чистая вода или сухие соли не могут сами по себе проводить электрический ток, в то время как водные растворы солей являются прекрасными проводниками. Аррениус исследовал прохождение электрического тока через многие типы растворов.

Хотя Сванте Аррениус по образованию - физик, он знаменит своими химическими исследованиями и стал одним из основателей новой науки - физической химии. Больше всего он занимался изучением поведения электролитов в растворах, а также исследованием скорости химических реакций. Начало работ Аррениуса, приведших к созданию теории электролитической диссоциации, относится к 1883 - 1884 г.г. Он изучал электропроводимость сильноразбавленных растворов электролитов, потому что они в то время были мало исследованы и потому, что в них молекула электролита имеет простор для своего свободного перемещения.
Молодой учёный рассуждал так: если некоторая часть из всех молекул электролита, растворённых в воде, проводит ток, то чем больше разведение, тем больше может появиться проводящих молекул и тем больше будет электропроводность раствора. А если так, то в растворе может происходить самопроизвольная, т.е. без воздействия тока, диссоциация электролита на активные молекулы.
«Эта мысль, - вспоминал впоследствии Аррениус, - явилась у меня в ночь на 17 мая 1883 г., и я не мог спать, пока не продумал всей проблемы». Сванте было в то время 24 года.
Аррениус поделился своими успехами со своим учителем профессором П.Т.Клеве. Он вспоминала: «Я сказал Клеве о том, что установил новую теорию химического действия электролитов». «Это же прямо замечательно», - сказал Клеве высокомерно иронически, показывая мне, что считает ниже своего достоинства вникать в такие смехотворные рассуждения».
В 1884 г. Аррениус представил в Упсальский университет докторскую диссертацию «Исследования гальванической проводимости электролитов». Аррениус пришел к следующим заключениям: сопротивление раствора электролита растет, если его разбавить; в сильно разбавленном растворе электропроводность пропорциональна концентрации; электропроводность раствора - сумма электропроводностей соли и растворителя; отклонение от этих закономерностей наблюдается лишь тогда, когда происходит реакция между веществом и растворителем.
Из этих фактов Аррениус сделал вывод, что молекула распадается на положительные и отрицательные фрагменты - ионы. Электрический ток направляет ионы к противоположно заряженным электродам. Эта гипотеза составила основу докторской диссертации Аррениуса. Иронически относившийся к этой работе П. Клеве через 20 лет поздравил Аррениуса с присуждением ему Нобелевской премии.

Хотя 26 мая 1884 г. Аррениус и защитил докторскую диссертацию, ему было отказано в должности доцента по физике в Упсальском университете: диссертация получила оценку «без похвалы» - университет не хотел скомпрометировать себя официальным приглашением в свои стены автора «сумасшедших» идей. В этой работе уже содержались основные положения теории электролитической диссоциации. Столь привычные в наши дни представления, что соли, кислоты и основания в водном растворе находятся в большей или меньшей степени в виде свободно движущихся ионов, по мнению химиков того времени, ниспровергали все ранее существовавшие взгляды. Поэтому вначале почти все ученые принимали теорию Аррениуса весьма сдержанно; многие в значительной мере скептически, а некоторые даже считали ее бессмыслицей
Несколько экземпляров своей диссертации С. Аррениус послал самым авторитетным в то время учёным: Р. Клаузиусу, Я.Вант-Гоффу, В.Оствальду и Л. Мейеру.

«Эти знаменитые люди, - писал Аррениус, - с которыми не могли сравниться даже приблизительно мои упсальские учителя, прислали мне такие ответы, как будто я был их коллегой, а не желторотым школьником».
На стипендию Академии наук Аррениус продолжает своё образование в лабораториях выдающихся европейских учёных. В 1886г. он работал в рижской лаборатории Оствальда, изучая электрическую проводимость водных растворов различных веществ. Эти исследования блестяще подтвердили основные положения докторской диссертации С.Аррениуса. Таким образом, уже через два года после создания теории электролитической диссоциации её положения оказали сильное стимулирующее действие на развитие химической кинетики. Теория С.Аррениуса находила всё больше сторонников главным образом среди молодых учёных. Оствальд и Вант-Гофф поддержали взгляды Аррениуса.
Дальнейшее развитие физики и химии показало правильность представлений С.Аррениуса. Первым научным отличием С.Аррениуса было избрание его в 1895 году почётным членом Германского электрохимического общества. Уже через год С.Аррениус становится ректором Высшей школы в Стокгольме. Научный авторитет С.Аррениуса был так велик, что много начинающих физико-химиков приезжали из других стран для работы в его лаборатории. В1901 году С.Аррениус был избран в Академию наук Швеции. С этого времени награды и почести начинают сыпаться на С.Аррениуса как из рога изобилия.
В 1886 году Аррениус получил стипендию Шведской королевской академии наук, это позволило ему совершить научное турне по Европе.

Вначале он приехал в Ригу. Поработав в лаборатории у Оствальда, он отправился в Вюрцбург, где стал учеником известного химика Фридриха Кольрауша, исследовал внутреннее трение разбавленных растворов и влияние света на электропроводность. Одновременно, он постепенно стал завязывать научные связи: он познакомился с Вальтером Нернстом, открывшим третий закон термодинамики (Нобелевская премия по химии 1920г.). Затем Аррениус переехал в Грац по приглашению Людвига Больцмана и уже на обратном пути провел несколько недель в Амстердаме, где находилась лаборатория Якоба Вант-Гоф-фа. В его лаборатории Аррениус увлекся исследованиями осмотического давления. Он хотел понять причину выравнивания концентраций двух разных растворов, разделенных тонкой мембраной.
С.Аррениус, Я.Г.Вант-Гофф и В.Оствальд - три «звезды» науки стояли у колыбели физической химии. В 1887 г. они основали «Журнал физической химии», в первом номере которого под общим заголовком «О диссоциации растворённых в воде веществ» были помещены статья Вант-Гоффа «Осмотическая теория растворов» и работа Аррениуса «Попытка расчёта констант диссоциации (коэффициентов активности) растворённых в воде веществ».

В статье «О диссоциации растворенных в воде веществ», опубликованной в конце 1887 г.. Аррениус сформулировал основные положения теории электролитической диссоциации:
электролиты в растворах состоят из частично диссоциированных молекул, количество которых растет при разбавлении раствора,
образующиеся при диссоциации молекул ионы определяют специфические физические и химические свойства растворов электролитов;
в бесконечно разбавленных растворах молекулы существуют только в виде ионов;
соединение в растворе тем более активно, чем больше оно диссоциировано на ионы.
На основании представлений об образовании активных частиц в растворах электролитов Аррениус выдвинул общую теорию образования "активных" молекул при химических реакциях.
Аррениус наметил пути изучения природы и вида температурной зависимости скорости реакции. При дальнейшем исследовании другими учеными (в первую очередь английским химиком У. Мак-Льюисом) в 1920—1930-х гг. было окончательно выведено уравнение этой зависимости, получившее имя Аррениуса. Оно стало одним из основных уравнений химической кинетики, а энергия активации — важной количественной характеристикой реакционной способности веществ.
Веселый и добродушный великан Сванте Аррениус, настоящий "сын шведской сельской местности", всегда был душой общества, располагал к себе коллег и просто знакомых. Он был дважды женат; его двух сыновей звали Олаф и Свен. Он получил широкую известность не только как физико-химик, но и как автор множества учебников, научно-популярных и просто популярных статей и книг по геофизике, астрономии, биологии и медицине.

Путь к мировому признанию для Аррениуса-химика был совсем не прост. Понадобились годы напряжённой работы, твёрдость убеждений, настойчивость в достижении цели, беспримерное трудолюбие и громадная выдержка. У теории электролитической диссоциации в ученом мире были очень серьезные противники. Они называли его и его сторонников «дикой армией ионистов». Так, Д.И. Менделеев резко критиковал не только саму идею Аррениуса о диссоциации, но и чисто "физический" подход к пониманию природы растворов, не учитывающий химических взаимодействий между растворенным веществом и растворителем.
Впоследствии выяснилось, что и Аррениус, и Менделеев были каждый по-своему правы, и их взгляды, дополняя друг друга, составили основу новой (протонной) теории кислот и оснований.
В 1888г. Аррениус посетил Макса Планка в Киле и работал у Вант-Гоффа в Амстердаме.
В 1894 году он женился на своей ассистентке Софье фон Рудбек. Через год у них родился сын Олеф. Однако их семейная жизнь не сложилась, и поэтому вскоре они расстались. Аррениус очень переживал из-за разлуки с сыном. В 1905 году он женился на Марии (Майе) Йоханссон, которая родила ему сына и двух дочерей.

Создав основные положения теории электролитической диссоциации, Аррениус показал её применимость в различных областях естество¬знания. За создание теории в 1903г. Аррениус был удостоен Нобелевской премии по химии «как факт признания особого значения его теории электролитической диссоциации для развития химии».
Выступая от имени Шведской королевской академии наук, X. Р. Тернеблад подчеркнул, что теория ионов Аррениуса заложила качественную основу электрохимии, «позволив применять к ней математический подход». «Одним из наиболее важных результатов теории Аррениуса, – сказал Тернеблад, – является завершение колоссального обобщения, за которое первая Нобелевская премия по химии была присуждена Вант-Гоффу».
Другим значительным вкладом Аррениуса в развитие естествознания было подробное физико-химическое рассмотрение теории токсинов и антитоксинов.
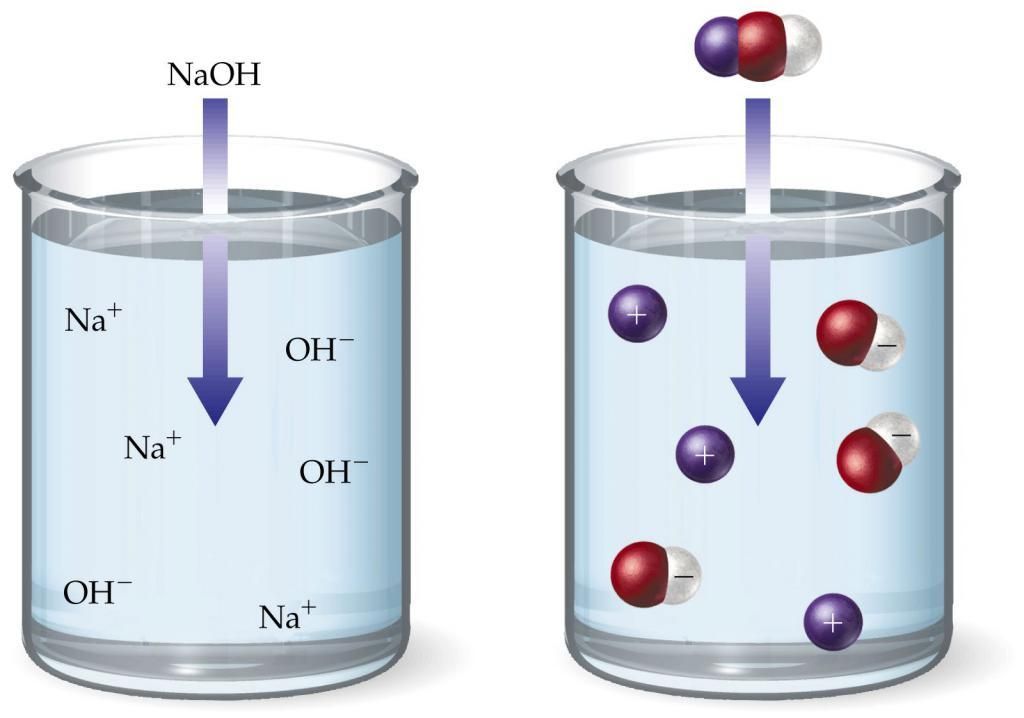
В это время Аррениус также изучает осмотическое давление. Осмотическое давление является механизмом стремления двух различных растворов по обе стороны мембраны к установлению определенной равновесной концентрации, не обязательно одинаковой. Вант-Гофф выразил осмотическое давление формулой PV = iRT, где Р обозначает осмотическое давление вещества, растворенного в жидкости; V - объем; R - давление любого присутствующего газа, Т - температуру и i - коэффициент, для газов часто равен 1, а для растворов, содержащих соли, - больше 1. Вант-Гофф не мог объяснить, почему изменяется значение i, а работа Аррениуса помогла ему показать, что этот коэффициент может быть связан с числом ионов, находящихся в растворе.
Аррениус изучал взаимосвязи между явлениями не только в химии. Ученый с широким диапазоном интересов, Аррениус проводил исследования во многих областях физики: опубликовал статью о шаровых молниях ( 1883), изучал влияние солнечной радиации на атмосферу, искал объяснение таким климатическим изменениям, как ледниковые периоды, пытался применить физико-химические теории к изучению вулканической активности. В 1901 году вместе с несколькими своими коллегами он подтвердил гипотезу Джеймса Клерка Максвелла о том, что космическая радиация оказывает давление на частицы.

Аррениус продолжил изучение проблемы и, используя это явление, предпринял попытку объяснить природу северного полярного сияния и солнечной короны. Он также предположил, что в космическом пространстве благодаря давлению света могут переноситься споры семян. В 1902 году начал исследования в области иммунохимии - науки, которая не переставала интересовать его в течение многих лет, изучал химические реакции в живых организмах, доказал, что нет принципиальной разницы между химическими реакциями in vitro и in vivo. Также он размышлял об искусственных языках, предложив собственную модификацию английского языка.
В 1903г. в двухтомном "Учебнике космической физики" - первом учебном пособии по этой научной дисциплине - он изложил результаты своих исследований основополагающих законов происхождения и развития небесных тел. Он отверг как явно ошибочные представления Платона и средневековых последователей Аристотеля, послужившие в своё время основой для возникновения алхимии и астрологии. Много сил было затрачено Аррениусом на борьбу с научными противниками и недоброжелателями.

В 1895г. Аррениус - профессор физики в Стокгольмском университете, а в 1899-1902 гг. - ректор этого университета. С 1905 по 1927 гг. он работал руководителем физико-химического отдела Нобелевского института Стокгольмской Академии наук. Английский химик Джеймс Уоркер вспоминал о нем так: «С момента его работы в Нобелевском институте жизнь его протекала очень спокойно. Из розовощекого парня он превратился в Швеции в научного оратора, известного и уважаемого всеми классами народа. В Аррениусе не было ничего академического. Сам он был крепко сложенным, светловолосым, голубоглазым и румяным, настоящим сыном шведской сельской местности. По характеру он был открытым, великодушным и экспансивным человеком. В нем было много здоровой энергии, первобытной силы. У него были сильные симпатии и антипатии, и под его врожденным добродушием и юмором таилась спящая драчливость, легко просыпавшаяся, когда затрагивались истина и свобода».
Горячо любивший свою родину Сванте Аррениус внёс немалый вклад в развитие экономики Швеции. В 1898г. на юбилее по случаю 50-летия со дня смерти великого Берцелиуса профессор Клеве в своей речи сказал: "Знамя, которое выпало из рук Й.Я. Берцелиуса после его смерти, сегодня снова поднято другим выдающимся шведским учёным - Аррениусом".
В статье "О диссоциации растворённых в воде веществ" (1887) Аррениус сформулировал основные положения теории электролитической диссоциации. Перечислим их:
I. электролиты в растворах состоят из частично диссоциированных молекул, количество которых растёт при разбавлении раствора;
образующиеся при диссоциации молекулы ионы определяют специфические физические и химические свойства растворов электролитов;
в бесконечно разбавленных растворах молекулы существуют только в виде ионов; соединение в растворе тем более активно, чем больше оно диссоциировано на ионы.
Дальнейшее изучение концентрированных растворов сильных электролитов и неводных растворов привело к созданию современного учения о растворах, которое не исключает теории Аррениуса, а расширяет и дополняет её новыми обобщениями.
В 1923 г. Аррениус высказал гипотезу, что основным источником энергии Солнца является энергия, выделяющаяся при термоядерной реакции образования гелия из водорода.
В Аррениусе не было ничего академического. Он был крепко сложенным, светловолосым, голубоглазым и румяным. По характеру был открытым, великодушным и экспансивным человеком. В нём было много первобытной силы. У него были сильные симпатии и антипатии, под его врожденным добродушием и юмором таилась спящая драчливость. Аррениус очень много работал, прихватывая и ночное время.
Обычно Аррениус поднимался на рассвете и с четырёх до восьми часов работал над рукописями. Непосильная нагрузка не могла не отразиться на его здоровье. В конце 1925 года у С.Аррениуса произошло кровоизлияние в мозг, в 1926 году врачи установили полное истощение. К работе он смог вернуться только через год. Однако в сентябре 1927 года болезнь возобновилась в ещё более острой форме.
2 октября 1927 года Аррениус умер в Стокгольме от острого кишечного катара. Похоронили учёного на родине в Упсале.
Всего Аррениус опубликовал около 200 научных статей и большое число книг. Исключительную популярность завоевала его книга "Возникновение мира".
Имя Аррениуса–писателя стало не менее известным, чем имена Жюля Верна и Майн Рида.
Сванте Аррениус принимал участие в полярной экспедиции в 1896 г. Он был в числе тех, кто встречал легендарную шхуну «Фрам» под управлением Нансена. Корабль возвращался из трёхлетнего плавания в арктических льдах.
По заданию шведского правительства он также занимался изучением вопроса о возможности технического использования водопадов для получения электроэнергии. Аррениус первым высказал теорию, что накопление в атмосфере углекислого газа способствует повышению средней температуры, то есть сформулировал гипотезу о парниковом эффекте.
Аррениус был удостоен многих наград и титулов. Среди них — медаль Дэви Лондонского королевского общества (1902), Нобелевская премия (1903), первая медаль Уилларда Гиббса Американского химического общества (1911), медаль Фарадея Британского химического общества (1914), медаль Франклина (1920). Он был членом Шведской королевской академии наук, иностранным членом Лондонского королевского общества и Германского химического общества. Удостоен почетных степеней многих университетов, в том числе Бирмингемского, Эдинбургского, Гейдельбергского, Лейпцигского, Оксфордского и Кембриджского.
Являлся иностранным членом-корреспондентом Петербургской академии наук (с 1903), почётным членом Академии наук СССР (с 1925).
Академик Н.Н.Семёнов писал: «Главное, что внёс в науку С. Аррениус, - теория электролитической диссоциации и представления об энергии активации и химических реакциях.Эти его открытия относятся к числу таких, которые составляют базу современной химии».
Рассказывают, что…
- С. Аррениус был учёным - энциклопедистом. Его интересовали проблемы жизни, естествознания, космической физики, иммунохимии. Как историк науки, он полагал, что его теория диссоциации проистекала из идей об атомах, получивших начало в Древней Греции.
